Covid-19: Anvisa analisa uso emergencial de medicação da Pfizer
As primeiras 24 horas de análise serão utilizadas para uma triagem do processo e verificar se os documentos necessários estão disponíveis. Se houver informações importantes faltando, a agência pode solicitá-las ao laboratório.
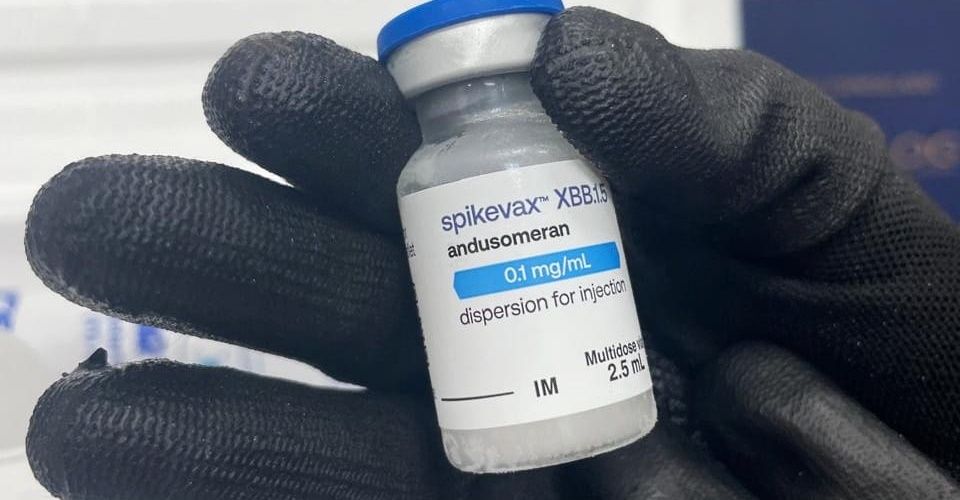
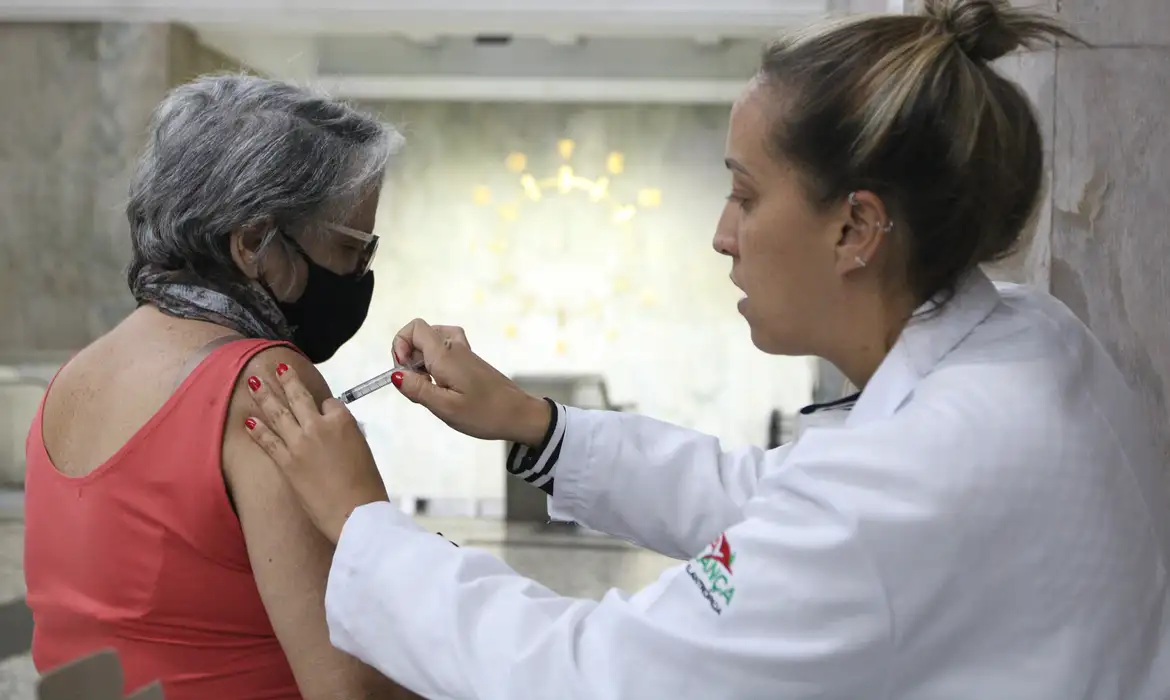
 Ilustrativa / Pixbay
Ilustrativa / PixbayA Agência Nacional de Vigilância Sanitária (Anvisa) recebeu, nesta quarta-feira (16/2), em Brasília, pedido da Pfizer para uso emergencial do medicamento contra Covid-19 Paxlovid (nirmatrelvir +ritonavir).
Segundo a farmacêutica, os estudos demonstram que, quando administrado no início da infecção, o Paxlovid, que é do tipo antiviral e de uso oral, tem a capacidade de reduzir os casos de hospitalização e mortes. Os dados serão analisados pela Anvisa.
“O prazo de avaliação para o uso emergencial e temporário de medicamento contra a covid-19 é de até 30 dias. A análise não considera o tempo do processo em status de exigência técnica, que é quando o laboratório precisa responder questões técnicas feitas pela agência no processo”, explicou a Anvisa, em nota à imprensa.
As primeiras 24 horas de análise serão utilizadas para uma triagem do processo e verificar se os documentos necessários estão disponíveis. Se houver informações importantes faltando, a agência pode solicitá-las ao laboratório.
No último dia 19 de janeiro, a Anvisa e o laboratório já haviam realizado reunião de pré-submissão do produto, etapa anterior ao envio formal do pedido pela empresa.
LEIA MAIS: Confira a programação da vacinação contra a Covid-19 desta quarta-feira em Salvador
Acompanhe todas as notícias sobre o novo coronavírus.
Acompanhe nossas transmissões ao vivo e conteúdos exclusivos no www.aratuon.com.br/aovivo. Nos mande uma mensagem pelo WhatsApp: (71) 99986-0003.